近期,我校动物医学学院徐世文教授团队针对硒及硒蛋白功能,在国际权威期刊《Advanced Science》(影响因子14.1)及《Journal of Advanced Research》(影响因子13.0)连续发表三项高水平研究成果,分别揭示了硒缺乏通过SELENOT/mtROS/NADPH轴诱导鸡骨骼肌双硫死亡的分子机制,硒缺乏通过GPX3/PIG3轴调控线粒体自噬驱动Th17细胞异常分化的分子机制,以及硒缺乏加剧三甲基氯化锡(TMT)诱导鸡胸腺铁死亡的分子机制。我校为三篇论文的唯一署名单位。徐世文教授、林洪金教授和徐童副教授为通讯作者,博士研究生刘欢逸、余挺挺、高红鑫分别为三项研究的第一作者。
研究一:揭示硒缺乏通过SELENOT/mtROS/NADPH轴诱导鸡骨骼肌双硫死亡
团队在《Advanced Science》期刊在线发表题为“Redox Cascade in Chicken Skeletal Muscle: SELENOT Suppression in Selenium Deficiency Triggers Disulfidptosis via mtROS-NADPH Dysregulation”的研究论文。第一作者刘欢逸,通讯作者徐童。
原文链接:https://doi.org/10.1002/advs.202507283

骨骼肌萎缩主要表现为肌肉质量和肌纤维数量的双重下降。这一现象不仅困扰着人类的健康老龄化,也给养殖业带来了沉重的经济负担。硒蛋白T(SELENOT)是调控细胞氧化还原稳态的核心因子,但其在骨骼肌中的具体功能机制仍有待深入解析。
研究团队通过构建硒缺乏鸡模型和原代鸡骨骼肌细胞,综合运用转录组学、蛋白质组学、免疫荧光和分子生物学技术,系统揭示了SELENOT在调控骨骼肌双硫死亡中的关键作用。SELENOT缺乏损害线粒体呼吸链功能,导致线粒体活性氧(mtROS)过量产生、葡萄糖代谢重编程以及NADPH代谢紊乱。这些变化引起胱氨酸积累和双硫死亡,进而导致肌动蛋白二硫键异常结合。研究证实,TEMPO介导的mtROS抑制或补充 NADPH可部分逆转硒缺乏诱导的肌肉萎缩。SELENOT过表达能够有效缓解硒缺乏细胞中的氧化还原失衡、NADPH功能障碍、双硫死亡和肌管萎缩,而Rotenone诱导的mtROS激活或抑制NADPH的合成则逆转这些保护效应。
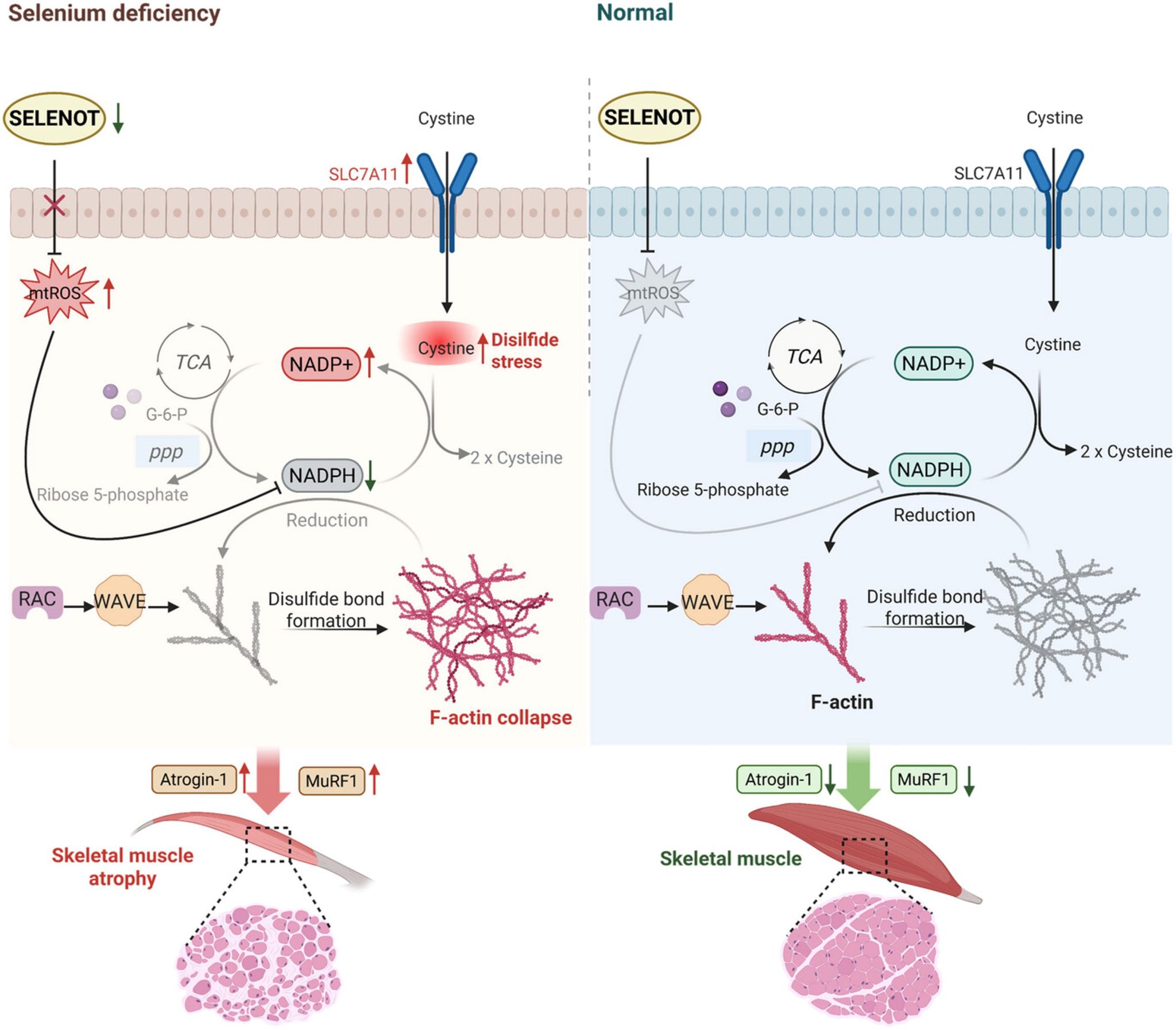
本研究确立了SELENOT/mtROS/NADPH轴在硒缺乏诱导肌肉萎缩中的关键作用,为肌肉消耗性疾病提供机制见解。该发现系统阐明SELENOT在硒缺乏诱导肌肉萎缩中的作用机制,不仅有助于揭示肌肉消耗性疾病的病理基础,也将为开发靶向治疗策略提供重要理论依据。
研究二:揭示硒缺乏通过GPX3/PIG3轴调控线粒体自噬进而驱动Th17细胞异常分化
团队在《Journal of Advanced Research》期刊在线发表题为“A novel mechanism of selenium deficiency driving aberrant Th17 cell differentiation via GPX3-targeted PIG3: mitophagy blockade exacerbates mtDNA release”的研究论文。第一作者余挺挺,通讯作者徐世文。
原文链接:https://doi.org/10.1016/j.jare.2026.02.043

Th17细胞是CD4⁺T细胞分化的重要亚群,其异常活化与多种自身免疫疾病的发病机制密切相关。流行病学研究和动物实验表明,硒缺乏与免疫功能抑制、免疫器官萎缩及自身免疫性疾病易感性增加密切相关,但其通过调控特定硒蛋白影响Th17细胞分化的机制尚不明确。
研究团队通过系统的体内外实验,发现硒缺乏能够显著下调GPX3蛋白表达并抑制PIG3活性,且GPX3与PIG3存在直接的蛋白互作关系。在动物实验中,硒缺乏通过下调猪脾组织中GPX3及其靶蛋白PIG3的表达,引发氧化还原失衡与线粒体功能障碍,进而导致线粒体融合-分裂失衡及线粒体自噬流受阻。这种自噬阻滞阻止了线粒体DNA(mtDNA)的有效清除,造成mtDNA在胞质内蓄积,并激活cGAS-STING信号通路,最终驱动Th17细胞异常分化。而过表达PIG3则可显著缓解由GPX3敲低引起的线粒体功能障碍,减少mtDNA泄漏并抑制Th17异常分化,且该保护作用严格依赖于完整的线粒体自噬流。由此,研究提出硒缺乏诱导免疫紊乱的核心机制为:通过抑制GPX3/PIG3轴导致线粒体自噬阻滞,加剧mtDNA渗漏,最终形成“线粒体功能障碍→mtDNA释放→Th17分化”的免疫失衡链条。
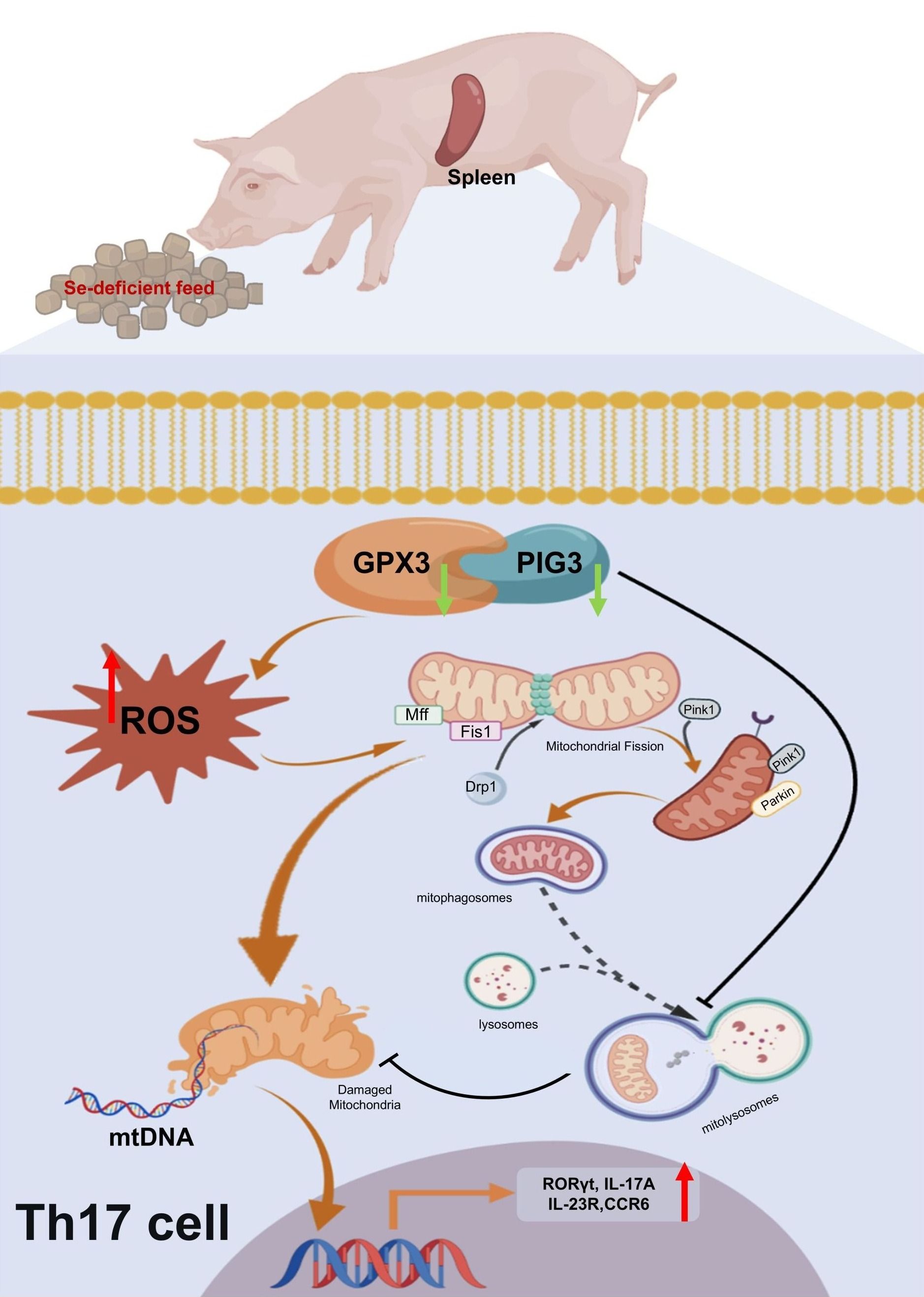
本研究从分子层面完整阐明了硒缺乏通过GPX3/PIG3轴调控Th17细胞分化的免疫机制,揭示了GPX3/PIG3信号轴在硒缺乏相关免疫失衡中的核心作用。同时,该研究从营养代谢与免疫调控的交叉视角出发,为硒缺乏相关免疫疾病及Th17驱动的炎症与免疫代谢性疾病的防治提供了新的理论依据。
研究三:揭示硒缺乏通过miR-7480-5p/SIRT3/GSH轴加剧TMT诱导的鸡胸腺铁死亡
团队同期在《Journal of Advanced Research》期刊在线发表题为“miR-7480-5p/SIRT3/GSH Axis Mediates Selenium Deficiency-Exacerbated Trimethyltin Chloride-Induced Ferroptosis in Chicken Thymus”的研究论文。第一作者高红鑫,通讯作者林洪金、徐童。
原文链接:https://doi.org/10.1016/j.jare.2026.03.043

三甲基氯化锡(TMT)是一种广泛存在于土壤、水体及养殖环境中的有机锡污染物,具有强免疫毒性,可造成胸腺萎缩和免疫功能下降。硒缺乏同样可导致免疫功能障碍。而我国大面积农业区域存在土壤硒缺乏问题,而硒缺乏与TMT联合暴露对家禽免疫器官的协同损伤效应及其分子机制此前尚不明确。
研究团队以AA肉鸡为研究模型,通过体内外实验发现,硒缺乏可显著加剧TMT诱导的胸腺组织结构异常、线粒体氧化应激、线粒体稳态失衡和功能障碍、线粒体自噬及铁死亡。进一步研究发现,线粒体氧化应激及线粒体自噬可调控铁死亡的发生,且硒缺乏与TMT联合暴露所致的损伤程度远高于单一暴露组。研究揭示,miR‑7480‑5p/SIRT3/GSH轴是该过程的核心调控通路:硒缺乏与TMT暴露通过上调miR‑7480‑5p表达来抑制SIRT3,降低还原型谷胱甘肽(GSH)水平并破坏线粒体质量控制,从而诱发线粒体过度自噬与铁死亡,最终导致胸腺免疫功能紊乱。
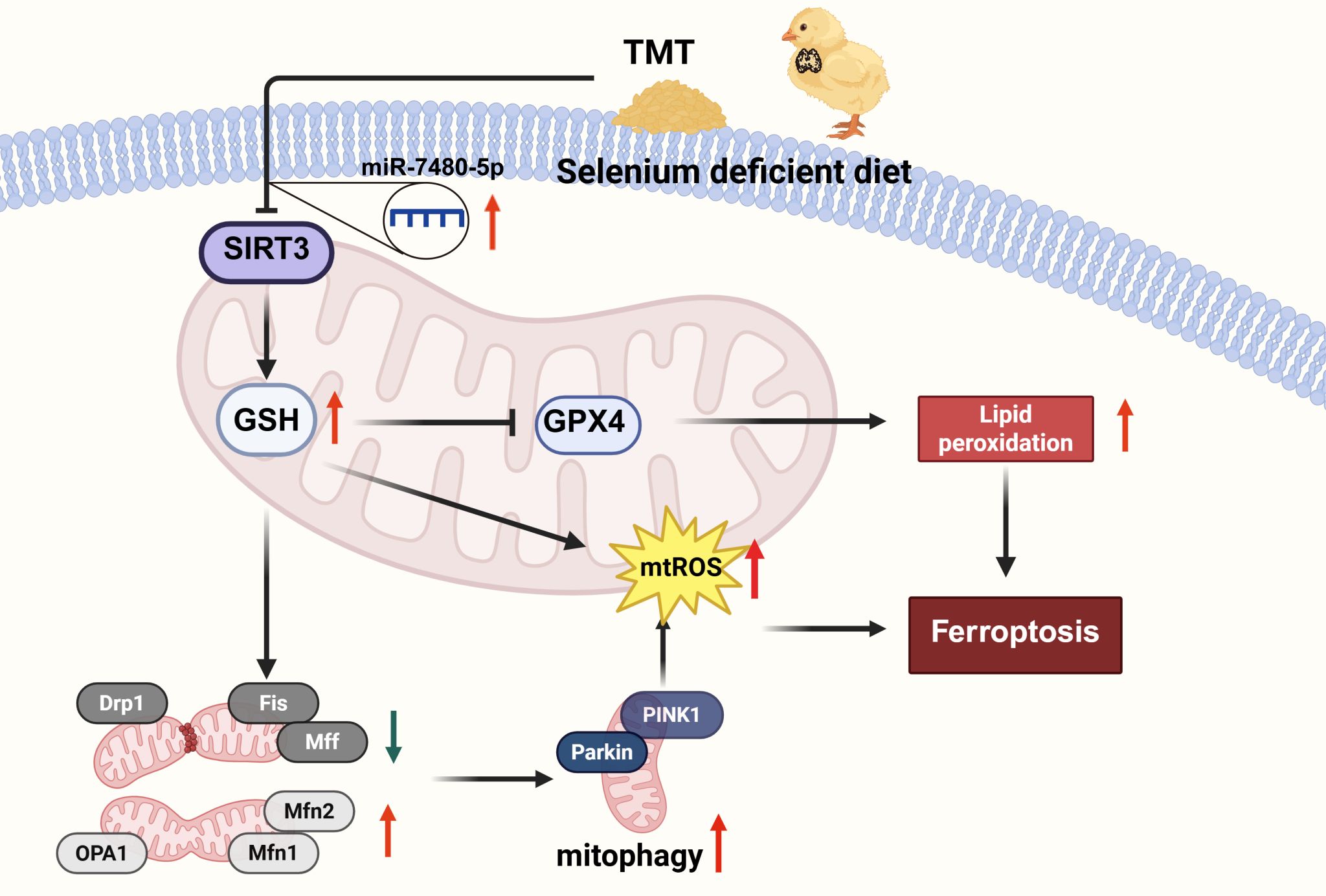
本研究首次揭示了硒缺乏与TMT联合暴露通过miR-7480-5p/SIRT3/GSH轴诱导线粒体功能障碍及铁死亡的分子机制,明确了硒缺乏加重TMT免疫毒性的关键分子靶点。这一发现为阐明缺硒地区TMT污染的联合毒性机制及开发干预措施提供了新靶点,也为低硒地区家禽健康养殖和环境污染物风险防控提供了科学依据与技术路径。
《Advanced Science》是Wiley旗下Advanced系列旗舰期刊,为完全开放获取的跨学科科学期刊,主要刊载材料科学、物理学、化学、医学、生命科学、环境科学、工程及社会科学等领域的前沿基础与应用研究成果。该刊年最新影响因子为14.1,5年平均影响因子15.6,在 2025年中科院期刊分区表中入选综合类期刊一区TOP,JCR Q1。
《Journal of Advanced Research》期刊是由Cairo University主办、Elsevier出版的综合性国际期刊,最新影响因子为13.0,位列中科院大类综合性期刊一区TOP期刊,JCR Q1,是国际多学科领域的高水平权威期刊。
上述三项研究工作得到了国家自然科学基金区域创新发展联合基金重点项目(U22A20524)及黑龙江省自然科学基金重点项目(ZD2023C002)的资助与支持。
(供稿/动物医学学院)




